政策红利释放|31类医疗器械分类调整,德为医疗助力行业创新升级
发布时间:
2026-01-29 11:01
2026年1月4日,国家药品监督管理局正式发布医疗器械分类调整公告,对涉及10个子目录的31类医疗器械实施优化分类调整,涵盖微创介入、康复辅助、医用耗材等多个热门领域。此次分类调整紧扣“风险适配、科学监管、促进创新”的核心原则,既进一步完善医疗器械监管体系、切实保障公众用械安全有效,也针对性为医疗器械行业创新发展松绑减负,尤其为聚焦微创介入领域的创新企业扫清发展障碍,释放出明确的政策扶持红利,推动行业高质量发展迈入新阶段。

图源国家药品监督管理局官网
此次医疗器械分类调整的核心亮点集中体现在三个方面,每一项调整都精准对接行业发展需求、贴合企业实际痛点。一是低风险产品降类减负,明确将输送导引器、手动轮椅车等此前属于二类的低风险产品,分别调整为一类或二类备案管理,大幅简化注册审批流程、缩短注册周期,降低企业合规成本和研发投入,助力这类临床常用产品快速落地市场、服务广大患者。二是高风险产品精准管控,针对微创介入、体外诊断等领域的高风险产品,进一步细化分类标准、明确产品归属,强化全流程监管要求,有效规避监管漏洞,保障高风险医疗器械的临床使用安全。三是分类标准向国际化靠拢,全面参考国际医疗器械监管机构论坛(IMDRF)的分类标准,统一分类口径,减少国产医疗器械跨国注册的技术壁垒和审批障碍,助力国产优质器械走出国门、参与全球市场竞争。值得关注的是,对于微创介入类器械企业而言,分类调整不仅加速了创新产品的迭代节奏,更对产品的测试验证提出了更高要求,而精准的测试验证正是产品合规上市、抢占市场的关键,西安德为医疗凭借自身技术优势,恰好为这类企业提供了全方位、专业化的支撑服务。
德为医疗产品获市场好评
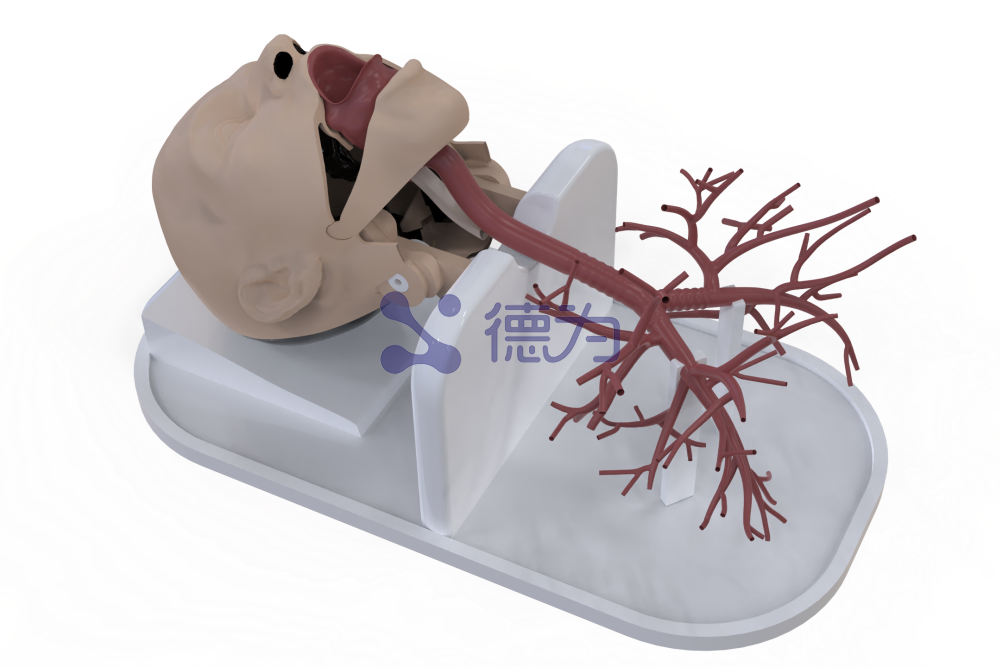
作为高端医学测试设备与解决方案的领军企业,西安德为医疗始终聚焦医疗器械工程师的仿真测试核心需求,深耕医学仿真与测试系统开发领域多年,积累了深厚的技术积淀和丰富的行业经验。针对微创介入类医疗器械的测试需求,德为医疗打造的核心仿真模型严格按照人体解剖结构一比一还原,其中血管模型采用自主研发的高透明软硅胶材料,不仅在外观上与人体血管高度契合,更能精准还原人体血管的弹性、韧性以及血流动力学特性,模拟临床实际手术场景中的各类复杂工况。同时,该仿真测试系统搭配高精度传感器、实时流量及压力监测仪、推送力测试装置等全套辅助设备,可实现对微创介入类医疗器械(如支架、导管、导丝等)的精准测试,涵盖产品性能、安全性、兼容性等多个核心维度,为企业提供从测试方案设计、测试设备调试到测试报告出具的“交钥匙”测试解决方案。借助这套专业的测试系统,企业可高效完成产品研发过程中的性能验证和合规检测,精准契合此次分类调整后的各项合规要求,大幅缩短产品研发周期、降低研发风险,加快创新产品的上市节奏,帮助企业快速抢抓政策红利、抢占市场先机。
德为医疗产品展示
此次31类医疗器械分类调整,并非简单的类别变更,本质上是国家推动医疗器械行业向“创新高效、合规可控、国际化发展”转型的重要举措,既为行业发展划定了清晰的监管边界,也为创新企业提供了广阔的发展空间。未来,随着分类调整政策的全面落地实施,医疗器械行业将迎来新一轮的创新升级浪潮,微创介入等热门领域的竞争也将日趋激烈,而精准的测试验证、过硬的产品质量将成为企业核心竞争力的关键。西安德为医疗将持续发挥自身在医学仿真、测试系统开发领域的技术优势,不断迭代升级产品和服务,持续为微创介入类器械企业、高端科研实验室提供专业、高效、精准的测试支撑,助力行业企业抢抓政策红利、突破技术瓶颈,推动我国医疗器械行业实现高质量创新升级,助力国产医疗器械在国内外市场实现更大突破。
关键词:
3D打印,医疗器械,微创介入,测试设备,测试系统,医学仿真,药品监督管理局,神经介入,硅胶血管模型
在线留言
*请保持您的电话畅通,我们将在24小时内与您取得联系
















 18192027578
18192027578